Supraventrikulære og intraventrikulære ledningsdefekter ved myokardiskemi og -infarkt
Ledningsforstyrrelser forårsaket av myokardiskemi og -infarkt
Bradykardi og ledningsforstyrrelser, som grenblokk, fascikulært blokk og atrioventrikulært (AV) blokk, utgjør hyppige og potensielt livstruende komplikasjoner ved myokardiskemi og akutt hjerteinfarkt. Disse tilstandene kan manifestere seg som direkte iskemiske tegn eller som konsekvenser av autonom ubalanse, og det er avgjørende for klinikeren å identifisere dem raskt. For å forstå patofysiologien og de prognostiske implikasjonene ved iskemi i ledningssystemet, kreves inngående kunnskap om den vaskulære anatomien. Figur 1 illustrerer de relevante delene av ledningssystemet og deres tilhørende blodforsyning.
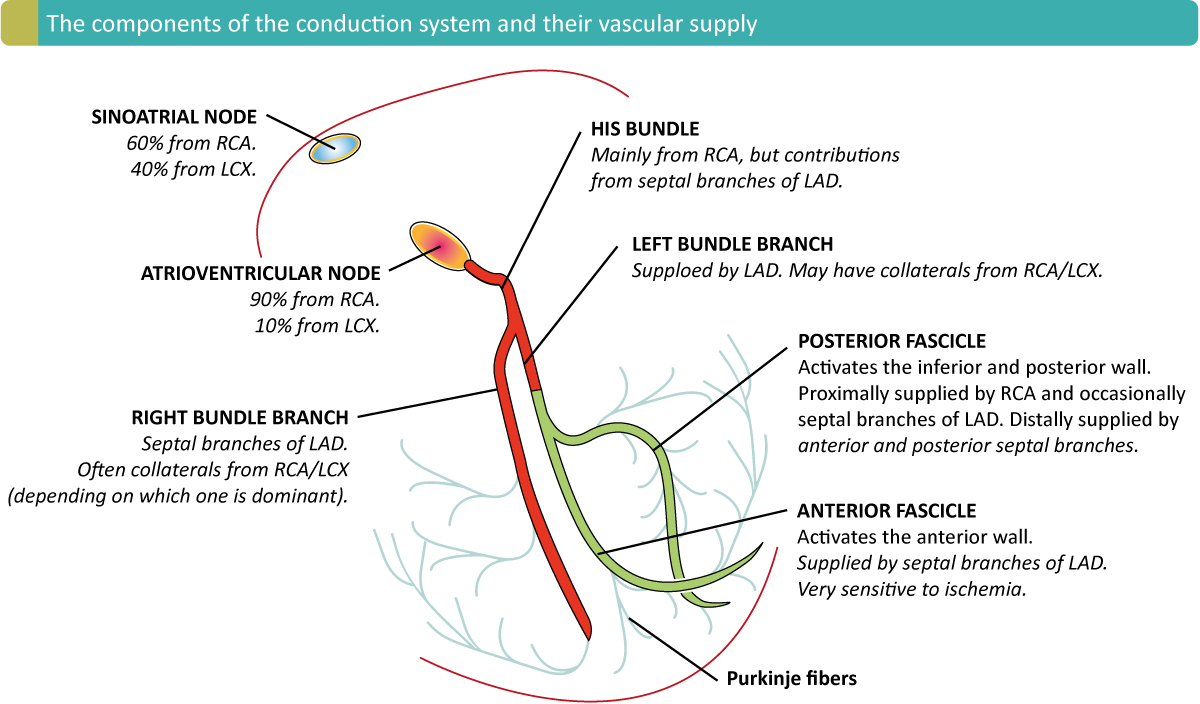
Arteriell blodforsyning av ledningssystemet
Figur 1 gir en skjematisk oversikt over ledningssystemets komponenter og deres arterielle blodforsyning, noe som er essensielt for å forutsi komplikasjoner ved okklusjon i ulike koronarkar. Sinusknuten forsynes oftest av RCA (ca. 60 %), mens den hos de resterende forsynes av LCX. AV-knuten mottar sin blodforsyning fra arteria nodi atrioventricularis, som hos 90 % av befolkningen avgår fra RCA.
His-bunten har en dobbel blodforsyning fra både RCA (via AV-nondalarterien) og LAD (via septale grener), noe som gjør den relativt motstandsdyktig mot iskemi. Grenbuntene har imidlertid mer spesifikk forsyning:
- Høyre grenbunt (RBB): Den proksimale delen forsynes av septale grener fra LAD, men kan også motta kollateraler fra RCA/LCX. Den første tredjedelen løper subendokardielt og kan delvis motta oksygen via diffusjon fra ventrikkelhulen. Deretter dykker den intramyokardielt før den igjen løper subendokardielt distalt. Det er viktig å merke seg at RBB ikke avgår grener i septum, men først ved moderatorbåndet og den fremre papillarmuskel.
- Venstre grenbunt (LBB): Hovedstammen forsynes av LAD (septale perforanter), men har ofte kollateral forsyning. Den deler seg i fremre og bakre fascikkel. Den fremre fascikkelen (forsynt av LAD) er tynn og sårbar, mens den bakre fascikkelen (forsynt av både LAD og PDA fra RCA/LCX) er tykkere og bredere, og dermed mer robust mot iskemisk skade.
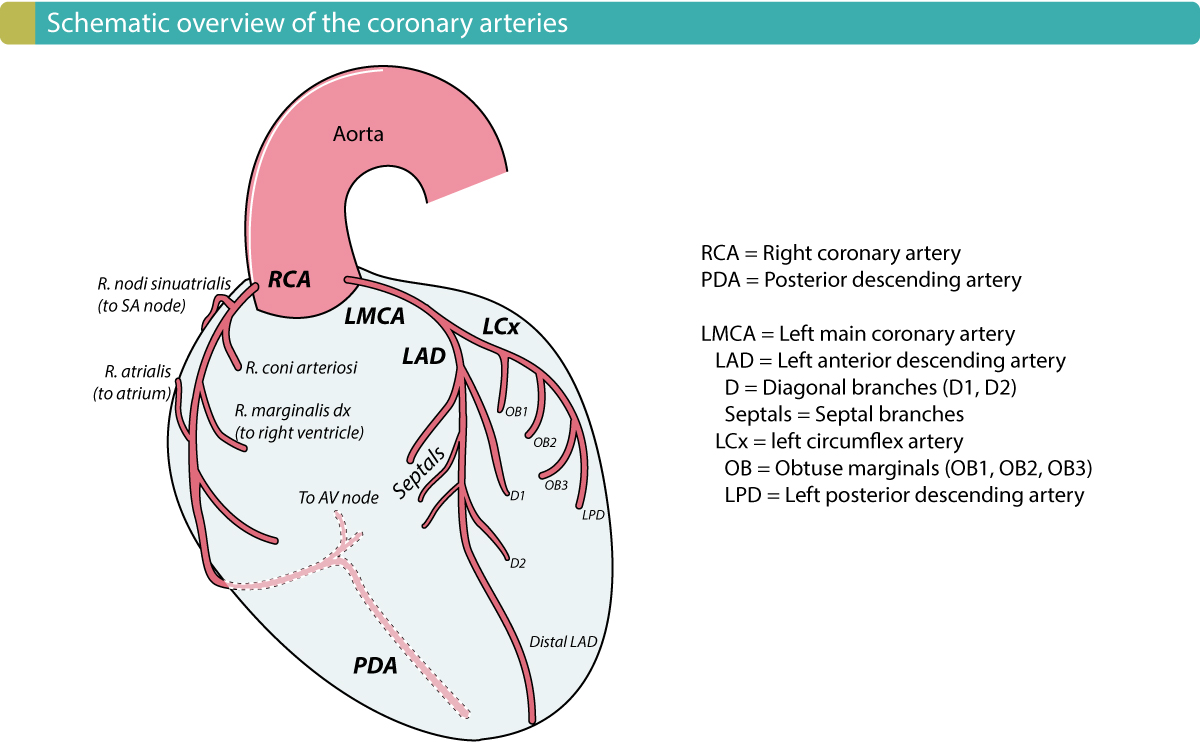
Koronararteriedominans
Begrepet koronardominans refererer til hvilken arterie som avgir arteria coronaria posterior descendens (PDA), som forsyner diafragmaflaten av venstre ventrikkel og bakre del av septum. Et høyredominant system innebærer at PDA avgår fra høyre koronararterie (RCA). Et venstredominant system innebærer at PDA avgår fra venstre cirkumfleks koronararterie (LCX). Høyredominant system er den klart vanligste anatomien, og forekommer hos ca. 85–90 % av alle individer. Dette har klinisk betydning, da en okklusjon i en dominant RCA vil kunne gi omfattende inferior iskemi og samtidig affisere blodforsyningen til AV-knuten, med påfølgende AV-blokk.
Grenblokk (Bundle Branch Block)
Grenblokk kan oppstå akutt som følge av myokardiskemi og infarkt, og representerer ofte proksimale okklusjoner med affeksjon av store myokardområder. Et nyoppstått grenblokk hos en pasient med typiske brystsmerter er en sterk indikasjon på pågående transmural iskemi. Prevalensen av høyre (RBBB) og venstre (LBBB) grenblokk ved ankomst hos pasienter med akutt hjerteinfarkt er henholdsvis ca. 6 % og 7 %. En andel av disse pasientene har nytt grenblokk. Historisk har nytt venstre grenblokk vært en direkte indikasjon for akutt koronarangiografi, men nyere retningslinjer (ESC) sidestiller nå også nyoppstått høyre grenblokk med vedvarende iskemiske symptomer som en STEMI-ekvivalent.
Tilstedeværelsen av grenblokk, spesielt LBBB, kompliserer EKG-tolkningen av iskemi. Dette fører ofte til at pasienter med grenblokk mottar reperfusjonsbehandling senere enn de med tydelige ST-elevasjoner, noe som kan bidra til dårligere prognose. Pasienter med grenblokk ved innleggelse har generelt høyere mortalitet, både intrahospitalt og på lang sikt, sammenlignet med pasienter med smale QRS-komplekser.
Det er også verdt å merke seg at pasienter med iskemisk hjertesykdom og høyre grenblokk ofte har et samtidig fascikulært blokk (bifascikulært blokk). Den venstre fremre fascikkelen er mest utsatt, da den deler blodforsyning med høyre grenbunt fra septale grener av LAD. Isolerte fascikulære blokk forekommer, men er sjeldnere ved akutt infarkt uten samtidig grenblokk.
Venstre grenblokk (LBBB)
Ved komplett venstre grenblokk endres ventrikkelens depolariseringsmønster fundamentalt, noe som gir sekundære ST-T-forandringer som maskerer typiske infarkttegn. Venstre grenblokk og iskemi/infarkt er omtalt i detalj i en egen artikkel. Det er likevel verdt å nevne Sgarbossa-kriteriene (og de modifiserte Smith-Sgarbossa-kriteriene), som er spesifikke verktøy for å identifisere akutt koronarokklusjon til tross for tilstedeværelsen av LBBB.
Høyre grenblokk (RBBB)
Høyre grenblokk påvirker primært den terminale delen av QRS-komplekset, og resulterer i en sekundær R-bølge (R’) i V1-V3 samt en bred og dyp S-bølge i V5-V6. Fordi aktiveringen av venstre ventrikkel skjer normalt via venstre grenbunt, vil de initielle QRS-kreftene være bevart. Dette betyr at kriterier for patologiske Q-bølger kan anvendes selv ved RBBB.
Selv om RBBB gir sekundære ST-depresjoner og T-inversjoner i V1-V3, er disse repolariseringskreftene sjelden sterke nok til å fullstendig maskere massive iskemiske ST-elevasjoner fra venstre ventrikkel. Imidlertid kan RBBB redusere amplituden på ST-elevasjoner i fremre vegg, noe som kan føre til undervurdering av infarktets størrelse. De klassiske STEMI-kriteriene gjelder ved RBBB, men klinikeren må være årvåken.
Et viktig klinisk poeng er fenomenet pseudonormalisering. Dersom en pasient har kjent RBBB med forventede T-bølgeinversjoner i V1-V3, og plutselig presenterer med «normale» positive T-bølger i disse avledningene under brystsmerter, er dette et sterkt tegn på akutt iskemi (hyperakutte T-bølger som utligner inversjonen).
Som nevnt er RBBB ofte ledsaget av venstre fremre fascikkelblokk (LAFB) ved proksimale LAD-okklusjoner. Dette gir Q-bølger i V2-V3 og venstresidig akseavvik, men Q-bølgene kan være små. Denne kombinasjonen indikerer omfattende septal iskemi.
Nyere forskning, inkludert arbeidet til Widimsky et al (European Heart Journal), understreker at nyoppstått RBBB kan være en like sterk markør for akutt LAD-okklusjon og dårlig prognose som LBBB. Deres studier viste at sykehusdødeligheten for pasienter med nytt RBBB var sammenlignbar med, eller til og med høyere enn, for pasienter med nytt LBBB. Dette skyldes ofte at RBBB ved infarkt indikerer en stor proksimal okklusjon som truer store deler av myokard. Derfor bør nyoppstått RBBB i en klinisk setting med brystsmerter håndteres aggressivt, ofte med vurdering for umiddelbar angiografi.
Atrioventrikulære (AV) blokk og bradykardi
AV-blokk ved akutt koronarsyndrom oppstår enten som følge av autonom ubalanse (høy vagal tonus) eller grunnet direkte iskemisk skade på ledningsvevet. Skillet mellom disse to mekanismene er klinisk avgjørende, da prognose og behandling varierer betydelig avhengig av infarktets lokalisasjon (inferior vs. anterior).
Ledningsforstyrrelser ved inferior iskemi/infarkt
Ledningsforstyrrelser ved inferiort infarkt er vanlige, men har generelt god langtidsprognose. Sinusbradykardi forekommer hos opptil 40 % av pasientene, ofte i den hyperakutte fasen. Dette skyldes Bezold-Jarisch-refleksen, hvor iskemisk stimulering av vagale afferente fibre i inferiort myokard utløser kraftig parasympatisk aktivitet, som gir bradykardi og hypotensjon.
AV-blokk ved inferiort infarkt er oftest lokalisert i selve AV-knuten (supra-Hisisk blokk). Fordi AV-knuten er rik på vagal innervering, er disse blokkene ofte reversible og responderer på atropin. Tilstanden kan utvikle seg gradvis (Wenckebach-fenomen/Mobitz type I), og ved komplett blokk vil erstatningsrytmen (escape rhythm) vanligvis være smalspektret (QRS < 0,12 s) og ha en adekvat frekvens (40–60/min) fordi den genereres høyt i His-bunten.
Det finnes også en subakutt form for AV-blokk som skyldes ødem og akkumulering av adenosin i AV-knuteområdet. Denne oppstår gjerne etter 24 timer og er, i likhet med den akutte formen, forbigående, men responderer dårligere på atropin. Aminofyllin (adenosinantagonist) kan vurderes i sjeldne tilfeller, men er ikke standardbehandling.
Tabell 1. Ledningsdefekter ved iskemi/infarkt i inferiorveggen
| Defekt | Kommentar | Prognose |
| Sinusbradykardi | De vanligste komplikasjonene. Forekommer i opptil 40 % av tilfellene (Bezold-Jarisch-refleks). | Forårsakes av økt vagal tonus og er derfor forbigående. God prognose. |
| Dysfunksjon i sinusknuten | Mindre vanlig. Kan sees i den subakutte fasen (>24 timer). | Kan bli permanent, men krever sjelden pacemaker. |
| Førstegrads AV-blokk | Vanlig. | Majoriteten forsvinner spontant i løpet av dager. |
| Andregrads AV-blokk, Mobitz type 1 (Wenckebach) | Relativt vanlig ved inferiort infarkt. | God prognose. Går som regel tilbake. |
| Andregrads AV-blokk, Mobitz type 2 | Sjeldent ved inferiort infarkt. Typisk for fremre vegginfarkt. | Mer alvorlig, kan indikere større skade. |
| AV-blokk av tredje grad | Forekommer hos ca. 10 %. Vanligvis intranodal defekt med smal QRS erstatningsrytme. Utvikler seg ofte gradvis. | God reversibilitet. Sjelden behov for permanent pacemaker. |
Ledningsforstyrrelser ved fremre vegginfarkt
I kontrast til inferiort infarkt, er ledningsforstyrrelser ved anteriort infarkt et svært alvorlig tegn. Disse blokkene skyldes ikke vagal tonus, men omfattende nekrose av septum og ledningssystemet under His-bunten (infra-Hisisk blokk). Årsaken er nesten alltid en proksimal okklusjon i LAD, ofte før første septalavgang. Fordi skaden innebærer vevsdød, er blokkene ofte permanente.
Utviklingen er gjerne brå og ustabil. Et typisk forløp kan være utvikling av RBBB med venstresidig akseavvik (bifascikulært blokk), som raskt progredierer til Mobitz type II eller totalt AV-blokk. Erstatningsrytmen ved totalt blokk sitter distalt i ventriklene, gir brede QRS-komplekser, er langsom (< 40/min) og upålitelig (risiko for asystole). Atropin har ingen effekt på disse infra-Hisiske blokkene.
Kombinasjonen av trifascikulært blokk (f.eks. vekslende grenblokk eller bifascikulært blokk med forlenget PR-intervall) indikerer at alle tre fascikler er kompromittert, og risikoen for progresjon til totalt blokk er overhengende. Pasienter med fremre vegginfarkt og utvikling av høygradig blokk har svært høy mortalitet (opptil 80 % i eldre studier), primært grunnet omfattende myokardskade og pumpesvikt («power failure»), snarere enn selve rytmeforstyrrelsen.
Klinisk håndtering og behandling
Behandlingen av ledningsforstyrrelser ved akutt infarkt retter seg mot to mål: umiddelbar hemodynamisk stabilisering og revaskularisering av det iskemiske området.
- Medikamentell behandling: Ved symptomatisk sinusbradykardi eller AV-blokk ved inferiort infarkt, er atropin (0,5–1,0 mg i.v.) førstevalg. Ved manglende effekt kan isoprenalininfusjon forsøkes forsiktig, men vær oppmerksom på at dette øker myokards oksygenbehov og kan forverre iskemien.
- Midlertidig pacemaker: Transkutan pacing kan brukes i akuttfasen (beredskap), men er smertefullt for våkne pasienter. Transvenøs midlertidig pacemaker er indisert ved:
- Symptomatisk bradykardi refraktær mot medikamenter.
- Tredjegrads AV-blokk ved anteriort infarkt (uansett symptomer grunnet risiko for asystole).
- Mobitz type II blokk ved anteriort infarkt.
- Nytt grenblokk (bifascikulært) med forlenget PR-intervall kan vurderes for profylaktisk pacingelektrode.
- Revaskularisering: Rask PCI (eller trombolyse hvis PCI ikke er tilgjengelig) er den viktigste behandlingen for å begrense infarktstørrelsen og potensielt reversere iskemien i ledningssystemet.
- Permanent pacemaker: Vedvarende andre- eller tredjegrads AV-blokk etter revaskularisering er indikasjon for permanent pacemaker. Ved anteriort infarkt bør terskelen være lav hvis blokket persisterer, mens man ved inferiort infarkt ofte kan observere i opptil 5-7 dager da funksjonen ofte normaliseres.