Hjertets elektrofysiologi: aksjonspotensial, automatikk og vektorer
Hjertets elektrofysiologi: membranpotensial, aksjonspotensial, automatikk og elektriske vektorer
Hjertets pumpefunksjon er avhengig av en presis og koordinert elektrisk aktivering. Aksjonspotensialet utgjør den grunnleggende enheten for denne aktiviteten og består av en depolarisering (aktivering) etterfulgt av en repolarisering (gjenoppretting). Selv om fenomenet forekommer i alle hjerteceller, varierer morfologien og varigheten betydelig avhengig av celletype – fra de spesialiserte pacemakercellene til det kontraktile arbeidsmyokardet. Under depolarisering og repolarisering strømmer ioner (hovedsakelig Na⁺ [natrium], K⁺ [kalium] og Ca²⁺ [kalsium]) frem og tilbake over cellemembranen gjennom spesifikke ionekanaler. Ettersom ionene bærer elektrisk ladning, genererer deres bevegelse en transmembran strøm. Dette innebærer at forplantningen (spredningen) av aksjonspotensialet i realiteten tilsvarer spredningen av en elektrisk strøm gjennom et resistivt medium.
Alle vev og væsker som omgir hjertet, inneholder en høy konsentrasjon av elektrolytter, noe som gjør dem i stand til å fungere som volumledere. De elektriske feltene som genereres av summen av myokardiets celleaktivitet, ledes derfor gjennom kroppen til hudoverflaten, hvor potensialforskjeller kan registreres ved hjelp av elektroder. Elektrokardiografen (EKG-apparatet) registrerer og behandler disse signalene og fremstiller dem som et elektrokardiogram (EKG). Som nevnt tidligere er de elektriske potensialene i selve ledningssystemet (His-purkinje) for små til å kunne registreres med standard overflateelektroder; EKG-et representerer derfor primært massesummen av den elektriske aktiviteten i atriene og ventriklene.
Pacemakercellenes automatikk
Automatiseringen av cellene i sinusknuten er fundamentet for normal hjerterytme. Denne egenskapen forklares ved at disse cellene har et ustabilt hvilemembranpotensial. De begynner å «lekke» natriumioner (Na⁺) inn i cytoplasmaet så snart de vender tilbake til repolarisert tilstand (figur 1). Denne spontane diastoliske depolariseringen (fase 4) drives i stor grad av den såkalte «funny current» ($I_f$), en blandet innadgående strøm av natrium og kalium som aktiveres ved hyperpolarisering via HCN-kanaler (Hyperpolarization-activated Cyclic Nucleotide-gated channels).
Etter hvert som positive ioner strømmer inn, blir cellemembranen gradvis mer positiv. Når membranpotensialet når terskelverdien på ca. –40 mV, utløses et aksjonspotensial. I motsetning til arbeidsmyokardet, er oppstroket i sinusknutens aksjonspotensial (fase 0) avhengig av kalsium, ikke natrium. Ved –40 mV åpnes spenningsstyrte L-type kalsiumkanaler (Ca²⁺), slik at kalsiumioner strømmer inn og står for depolariseringen. Deretter åpnes utadrettede kaliumkanaler (K⁺), noe som fører til effluks av kalium og repolarisering av cellen (fase 3). Syklusen gjentar seg deretter (figur 1). Merk at helningen på pacemakerpotensialet i fase 4 avgjør hjertefrekvensen; sympatisk stimulering øker helningen (raskere fyring), mens parasympatisk stimulering reduserer den.
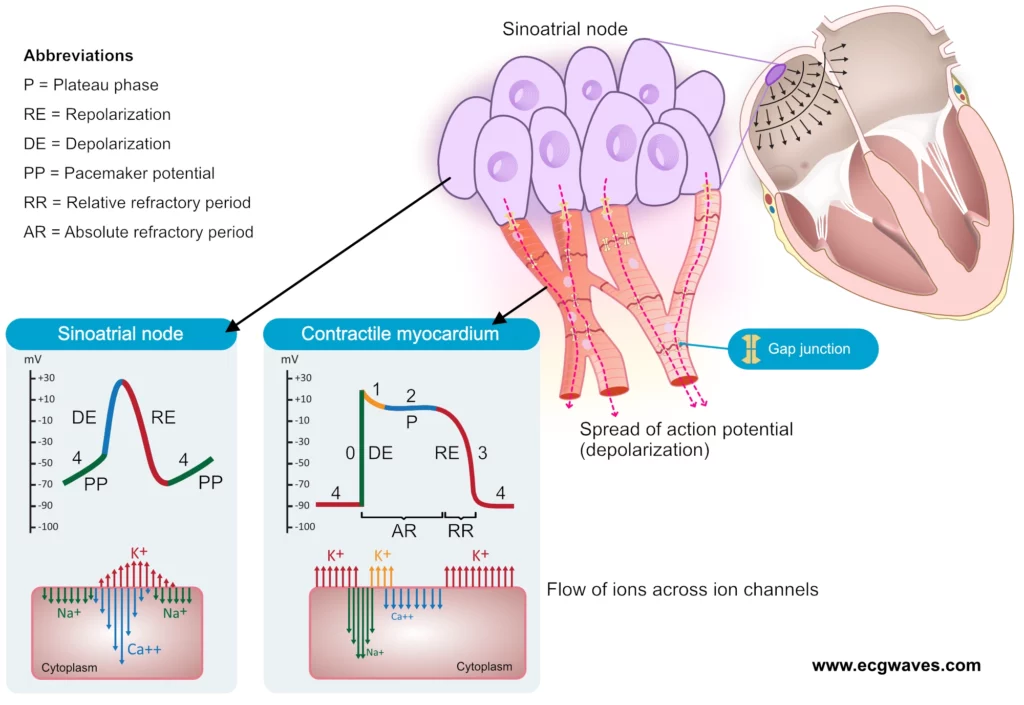
Depolariseringen sprer seg fra sinoatrialknuten til både atrie- og ventrikkelmyokard. Spredningen av aksjonspotensialet er mulig fordi alle hjertecellene er elektrisk koblet sammen via gap junctions (figur 1). Gap junctions er lavresistente proteinkanaler, bygget opp av connexiner, som forbinder cellemembranene til tilstøtende celler og tillater direkte ioneflyt mellom dem. Dette gjør at hjertet fungerer som et funksjonelt syncytium, hvor aksjonspotensialet overføres raskt fra celle til celle.
Variasjoner i typen og tettheten av connexiner bestemmer ledningshastigheten i vevet. Tettheten av gap junctions i Purkinje-nettverket er svært høy (samt høy forekomst av Connexin 40), noe som forklarer den raske impulsoverføringen (2–4 m/s) som sikrer synkron ventrikkelkontraksjon. I atrioventrikulærknuten er tettheten derimot svært lav (og dominert av Connexin 45), noe som resulterer i den fysiologiske forsinkelsen av impulsen. Overføringen av aksjonspotensialet mellom kontraktile myokardceller er moderat rask (ca. 0,5–1 m/s), begrenset av gap junctions i innskuddsskivene (intercalated discs).
Aksjonspotensialet i kontraktile celler
De kontraktile cellene (arbeidsmyokardet) har, i motsetning til cellene i sinoatrialknuten, et stabilt og svært negativt hvilepotensial (fase 4) på rundt –90 mV. Disse cellene må stimuleres av en nabocelle for å utløse et aksjonspotensial. Ved stimulering åpnes raske spenningsstyrte natriumkanaler (Na⁺), noe som fører til en massiv og rask innstrømning av natriumioner og depolarisering av cellen. De kontraktile cellene begynner å trekke seg sammen noen millisekunder etter at depolariseringen har startet, via en prosess kjent som eksitasjon-kontraksjon-kobling. Varigheten av aksjonspotensialet er omtrent 0,20 sekunder i atriemuskulaturen og 0,30–0,40 sekunder i ventrikkelmuskulaturen (figur 1).
Fasene er også illustrert i figur 1 ovenfor og kan beskrives detaljert som følger:
- Fase 4 (hvilefase): I hvilefasen er Na⁺-kanalene lukket, mens spesifikke kaliumkanaler ($I_{K1}$) er åpne. Effluks (utstrømning) av kalium ned sin konsentrasjonsgradient balanseres av den elektriske gradienten, og etablerer et negativt hvilemembranpotensial (ca. -90 mV), nær likevektspotensialet for kalium.
- Fase 0 (depolarisering): Ved elektrisk stimulering over terskelverdi åpnes de raske Na⁺-kanalene momentant. Dette gir en bratt stigning i membranpotensialet (raskt oppstrok) der cellen blir positivt ladet (overshoot til ca. +20 til +30 mV). Dette tilsvarer QRS-komplekset i EKG.
- Fase 1 (tidlig repolarisering): Na⁺-kanalene inaktiveres raskt. Samtidig åpnes en transient utadgående kaliumstrøm ($I_{to}$), som gir en kortvarig utstrømning av kalium. Dette gir en liten, rask repolarisering («notch») før platåfasen inntreffer.
- Fase 2 (platåfasen): Dette er den unike fasen for kardiomyocytter. Spenningsstyrte L-type kalsiumkanaler (Ca²⁺) åpnes, og kalsium strømmer inn i cellen. Denne innadgående positive strømmen balanseres av en utadgående strøm av kalium (via delayed rectifier channels, $I_{Kr}$ og $I_{Ks}$). Nettoresultatet er at membranpotensialet holder seg stabilt positivt i en lengre periode. Kalsiumet som strømmer inn trigger frigjøring av mer kalsium fra sarkoplasmatisk retikulum (Calcium-Induced Calcium Release), som er direkte ansvarlig for muskelkontraksjonen. Fase 2 tilsvarer ST-segmentet i EKG.
- Fase 3 (repolarisering): Kalsiumkanalene (Ca²⁺) lukkes gradvis, mens utstrømningen av kalium gjennom $I_{Kr}$ og $I_{Ks}$ øker, og etter hvert $I_{K1}$. Den dominerende utstrømningen av positive ioner bringer membranpotensialet raskt tilbake til hvilenivået på -90 mV. Fase 3 tilsvarer T-bølgen i EKG.
Klinisk relevans: Antiarytmika
Forståelsen av disse fasene er essensiell for bruken av antiarytmika, som ofte klassifiseres etter Vaughan Williams-systemet basert på hvilke kanaler de påvirker:
- Klasse I-midler (f.eks. flekainid) blokkerer Na⁺-kanaler i fase 0, noe som reduserer ledningshastigheten.
- Klasse III-midler (f.eks. amiodaron, sotalol) blokkerer K⁺-kanaler i fase 3, noe som forlenger repolariseringen og dermed aksjonspotensialets varighet (og QT-tiden).
- Klasse IV-midler (verapamil, diltiazem) blokkerer Ca²⁺-kanaler (fase 2 og sinusknutens fase 0/4).
Absolutte og relative refraktærperioder under aksjonspotensialet
Hjertemuskelcellenes evne til å reagere på nye impulser varierer gjennom syklusen. Under størstedelen av aksjonspotensialet (fra fase 0 til midten av fase 3) er myokardcellen i en absolutt refraktærperiode (ARP). Dette skyldes at natriumkanalene er i en inaktivert tilstand og ikke kan åpnes igjen før membranpotensialet er blitt tilstrekkelig negativt. Dette innebærer at et nytt aksjonspotensial ikke kan utløses, uavhengig av stimulusets styrke, noe som er en viktig beskyttelsesmekanisme mot tetaniske (vedvarende) kontraksjoner.
Denne perioden etterfølges av en relativ refraktærperiode (RRP), som varer gjennom siste del av fase 3. Her har noen Na⁺-kanaler gjenvunnet sin funksjon, men cellen er fortsatt delvis depolarisert. Et normalt stimulus vil ikke utløse et signal, men et tilstrekkelig kraftig stimulus kan initiere et nytt aksjonspotensial. Et slikt prematurt aksjonspotensial vil ofte ha lavere stigningshastighet og dermed langsommere ledning, noe som disponerer for re-entry arytmier. De absolutte og relative refraktærperiodene er illustrert i figur 2.
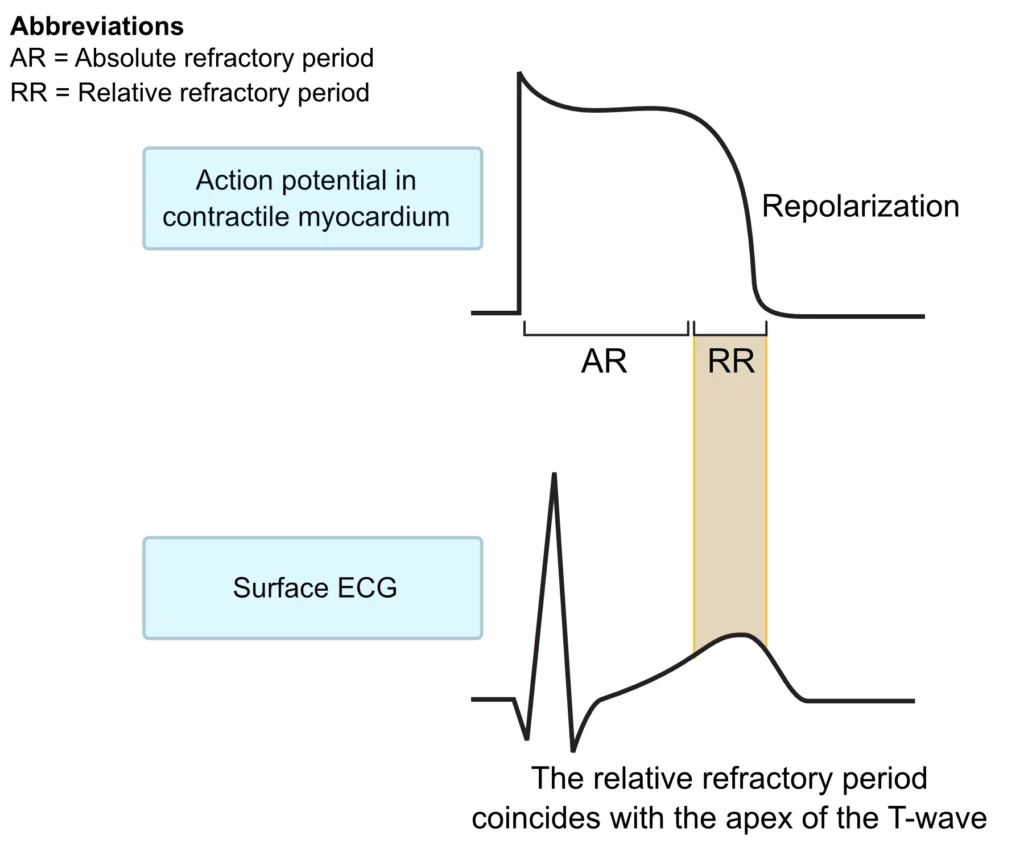
Som vist i figur 2 sammenfaller den relative refraktærperioden med toppen og slutten av T-bølgen. Denne fasen omtales tradisjonelt som en sårbar periode i hjertesyklusen. I dette tidsvinduet er det en heterogenitet i repolariseringen (noen celler er repolarisert, andre ikke), noe som skaper grobunn for ensrettet blokk og sirkelstrømmer (re-entry). Elektrisk stimulering her kan utløse et nytt aksjonspotensial som potensielt kan degenerere til livstruende ventrikulære arytmier, som ventrikkelflimmer.
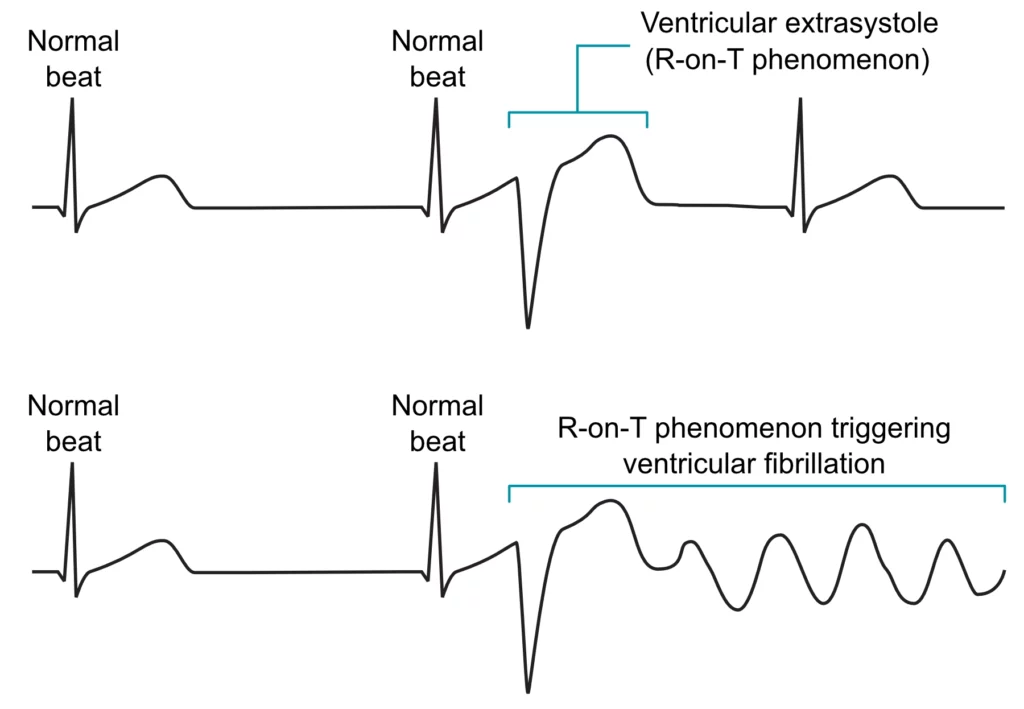
Slike hendelser forekommer tidvis i klinisk praksis. Stimulansen er som regel et prematurt ventrikulært slag (et ektopisk slag fra ventriklene) eller uhensiktsmessig stimulering fra en kunstig pacemaker som ikke har adekvat sensing. Når en ventrikulær depolarisering (R-bølge) faller sammen med T-bølgen fra forrige slag, omtales dette som et R‑on‑T‑fenomen. Det bør imidlertid understrekes at R‑on‑T‑fenomener er relativt hyppige ved vanlig ventrikulær ekstrasystoli, og at risikoen for ventrikkelflimmer er liten i et strukturelt normalt hjerte. Risikoen øker betraktelig dersom ventriklene er elektrisk ustabile, som ved akutt hjerteinfarkt (iskemi øker dispersjonen i repolarisering), elektrolyttforstyrrelser (hypokalemi), eller ved medfødt eller ervervet langt QT‑syndrom. Figur 3 viser to eksempler på R‑on‑T‑fenomenet.
Hva viser EKG-et?
Figur 4 viser de klassiske EKG-bølgeformene. Den første utslagsbølgen (heretter kalt bølge) er P-bølgen, som representerer atrieaktivering (depolarisering). Repolariseringen av atriene er vanligvis ikke synlig på overflate-EKG, ettersom den skjer samtidig med ventrikkelaktiveringen (depolariseringen), som genererer vesentlig større elektriske potensialer og derfor maskerer atrierespolariseringen («Ta-bølgen»). Ventrikulær depolarisering fremstår som QRS-komplekset, som består av tre bølger: Q, R og S. Variasjoner i retningen på disse bølgene skyldes endringer i retningen på de elektriske impulsene under ventrikulær depolarisering. T-bølgen representerer ventriklenes repolarisering.
Legg merke til den isoelektriske (rette) linjen mellom P-bølgen og QRS-komplekset (figur 4). Denne linjen kalles PR-segmentet (eller PQ-segmentet) og representerer impulsforsinkelsen i atrioventrikulærknuten (AV-knuten). Denne forsinkelsen er fysiologisk viktig for å la atriene tømme seg helt til ventriklene før ventrikkelkontraksjonen starter.
Det er avgjørende å forstå hvordan disse bølgeformene oppstår, noe som forutsetter kunnskap om de elektriske vektorene som er til stede gjennom hjertesyklusen. Vektorteori er et komplekst fagområde, og denne fremstillingen vil derfor ikke gå inn på de mest avanserte aspektene ved vektorløkker (vektorkardiografi), men konsentrere seg om de viktigste elektriske gjennomsnittsvektorene og deres innvirkning på EKG-kurven.
Elektriske vektorer
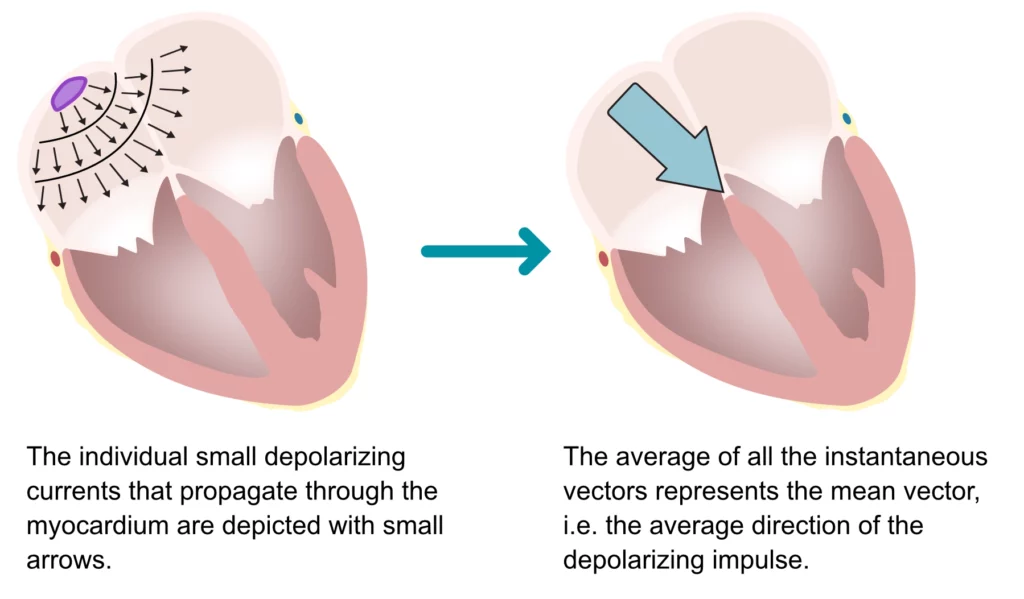
En vektor er en fysisk størrelse med både størrelse (magnitude) og retning i rommet. Bevegelsen av elektrisk ladede partikler – som oppstår under spredningen av hjertets aksjonspotensial – genererer en elektrisk dipol. Depolariseringen forplanter seg gjennom myokardiet på samme måte som en bølgefront sprer seg i vann. Til enhver tid finnes det mange små depolariserende bølgefronter som beveger seg i ulike retninger gjennom myokardiet (figur 5, venstre side). Vektorsummen (gjennomsnittet) av alle de individuelle bølgefrontene på et gitt tidspunkt representerer den elektriske hovedvektoren (figur 5, høyre side). Den elektriske vektoren angir dermed impulsens gjennomsnittlige retning og styrke. EKG-bølgeformene vist i figur 5 representerer projeksjonen av disse elektriske vektorene på EKG-avledningene.
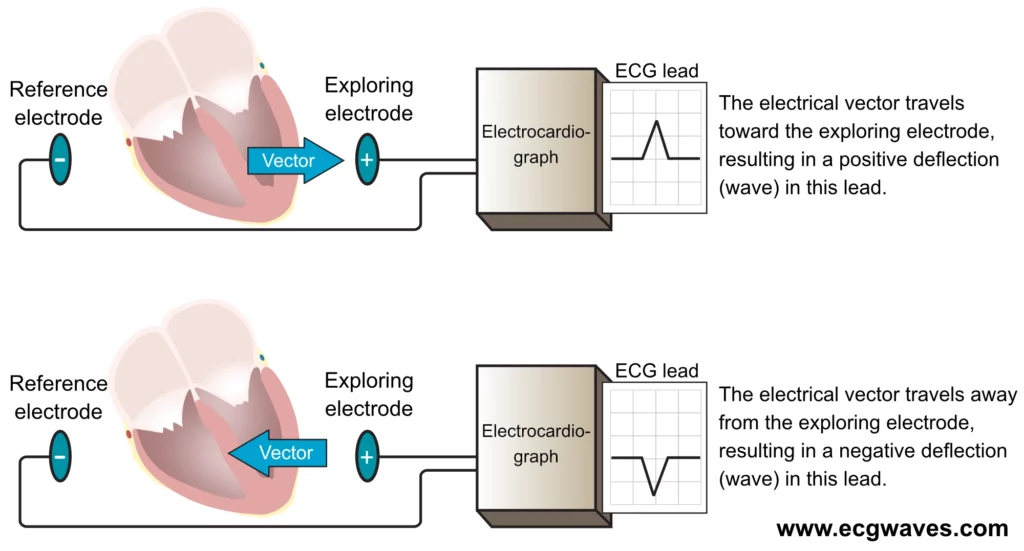
For å forstå hvordan en elektrisk vektor genererer en bølge på EKG-kurven, er det avgjørende å kjenne til hvordan EKG-avledningene er konstruert. Merk at avledningene (både bipolare og unipolare) vil bli gjennomgått i detalj i neste kapittel; her omtales kun aspekter som er relevante for elektriske vektorer. Elektrokardiografen (EKG-apparatet) bruker to elektroder til å beregne én EKG-kurve (figur 6) ved å sammenligne de elektriske potensialene registrert av hver elektrode. Den ene elektroden defineres som positiv (undersøkende elektrode/explorer), og den andre som negativ (referanseelektrode). Apparatet er konstruert slik at:
- En vektor som beveger seg mot den undersøkende elektroden, gir en positiv avbøyning (bølge) på EKG-kurven.
- En vektor som beveger seg bort fra den undersøkende elektroden, gir en negativ bølge (figur 6).
- En vektor som beveger seg vinkelrett på elektroden, vil gi liten eller ingen avbøyning (isoelektrisk).
Det er vanlig å si at den utforskende elektroden er den som «ser» hjertet, noe som kan gjøre tolkningen av EKG enklere. Den fysiologiske begrunnelsen for dette forklares nedenfor.
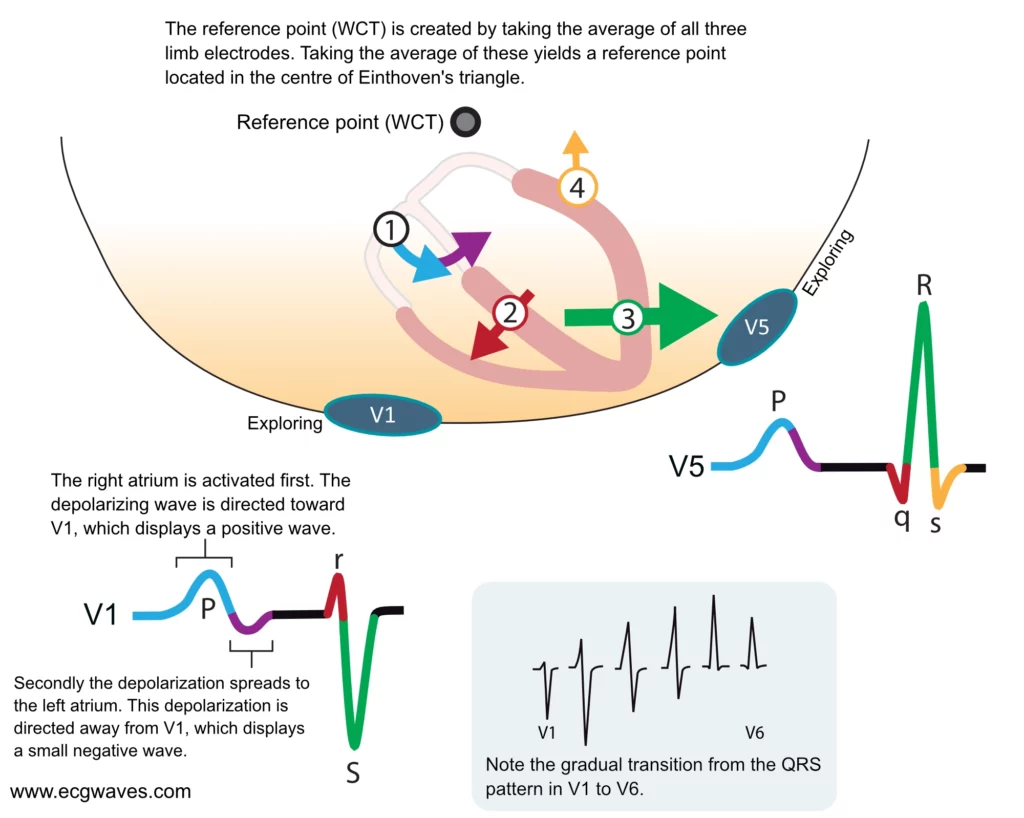
Nå som forholdet mellom elektriske vektorer og EKG-bølger er klarlagt, er det på tide å studere hjertets hovedvektorer og hvordan disse danner den klassiske EKG-kurven (QRS-morfologien). Avledningene V1 og V5 er valgt av pedagogiske grunner, da de primært registrerer vektorer som beveger seg i horisontalplanet. Dette skyldes plasseringen av den utforskende elektroden og referansepunktet. Den utforskende elektroden plasseres anteriort på brystveggen. Referansen er mer kompleks, ettersom den beregnes som gjennomsnittet av potensialene registrert fra lemelektrodene (høyre arm, venstre arm, venstre ben), noe som resulterer i et referansepunkt lokalisert inne i brystkassen (Wilsons sentrale terminal). Figur 7 illustrerer hvordan P-, Q-, R- og S-bølgene oppstår og fremtrer på EKG-kurven som et resultat av de fire hovedvektorene.
Den første vektoren: atriene
Den første vektoren stammer fra atrial depolarisering. Depolariseringen starter i sinoatrialknuten og sprer seg derfra som ringer i vann gjennom høyre atrium, deretter til venstre atrium. Under aktivering av høyre atrium er vektoren rettet anteriort, mot venstre og noe nedover. Når depolariseringen når venstre atrium, dreier vektoren mot venstre og noe bakover. Den atriale totalvektoren får dermed en svakt buet form (figur 7). Avledning V1 registrerer at den innledende vektoren (høyre atrium) beveger seg mot elektroden og viser derfor en positiv avbøyning, P-bølgen. V1 kan også registrere at vektoren beveger seg bort fra elektroden under aktivering av venstre atrium, noe som kan gi en liten negativ avbøyning i den terminale delen av P-bølgen (bifasisk P-bølge). En uttalt negativ terminal del i V1 er et spesifikt tegn på venstre atriumsbelastning. Avledning V5 registrerer derimot kun vektorer som beveger seg mot elektroden (om enn med varierende vinkler) under hele atrieaktiveringen, og viser derfor en jevnt positiv P-bølge.
Den andre vektoren: ventrikkelseptum (interventrikulær septum)
Ventrikkelseptumet er den første delen av ventriklene som depolariseres. Det mottar Purkinje-fibre fra venstre gren av His-bunten, og depolariseringen forløper derfor fra venstre side av septum mot høyre side. Den resulterende elektriske vektoren er rettet fremover og mot høyre. Siden ventrikkelseptumet er relativt lite, viser avledning V1 (som ligger til høyre) en liten positiv bølge (r-bølge), mens avledning V5 og V6 (som ligger til venstre) viser en liten negativ bølge (q-bølge, ofte kalt «septal q»). Det er altså den samme elektriske vektoren som gir opphav til r-bølgen i V1 og q-bølgen i V5/V6. Tap av denne septale vektoren kan sees ved venstre grenblokk (LBBB).
Den tredje vektoren: den frie ventrikkelveggen
Den neste og kraftigste vektoren oppstår ved den samtidige aktiveringen av de frie veggene i høyre og venstre ventrikkel. Totalvektoren er orientert mot venstre og nedover (figur 7). Dette kan forklares på følgende måte:
- Vektoren som oppstår ved aktivering av høyre ventrikkel (rettet mot høyre og fremover), er liten på grunn av høyre ventrikkels tynne vegg.
- Vektoren fra venstre ventrikkel (rettet mot venstre og bakover) er mange ganger større på grunn av den store muskelmassen.
- Resultatet er at vektoren fra høyre ventrikkel «drukner» i den dominerende vektoren fra venstre ventrikkel. Totalvektoren peker derfor mot venstre.
I tillegg er det viktig å merke seg at aktiveringen av ventrikkelens frie vegg går fra endokardiet til epikardiet. Dette skyldes at Purkinje-fibrene løper subendokardialt. Som vist i figur 7 er vektoren fra den frie ventrikkelveggen rettet mot venstre og noe nedover. Avledning V5 (som ser mot venstre ventrikkel) registrerer en kraftig vektor som beveger seg mot elektroden, og viser derfor en høy R-bølge. Avledning V1 (som ligger til høyre) registrerer en vektor som beveger seg bort, og viser dermed en uttalt negativ defleksjon, betegnet som S-bølge.
Den fjerde vektoren: basale deler av ventriklene
Den siste vektoren oppstår ved aktivering av de basale delene av ventriklene (hjertets base, nær atriene). Aktiveringen her skjer sist fordi det er færre Purkinje-fibre i dette området. Vektoren er rettet bakover, oppover og ofte mot høyre. Den beveger seg bort fra avledning V5, som dermed registrerer en negativ s-bølge. Avledning V1 registrerer vanligvis ikke denne vektoren tydelig, eller den inngår i slutten av S-bølgen eller kommer til syne som en liten r’-bølge.
Vektoren til T-bølgen
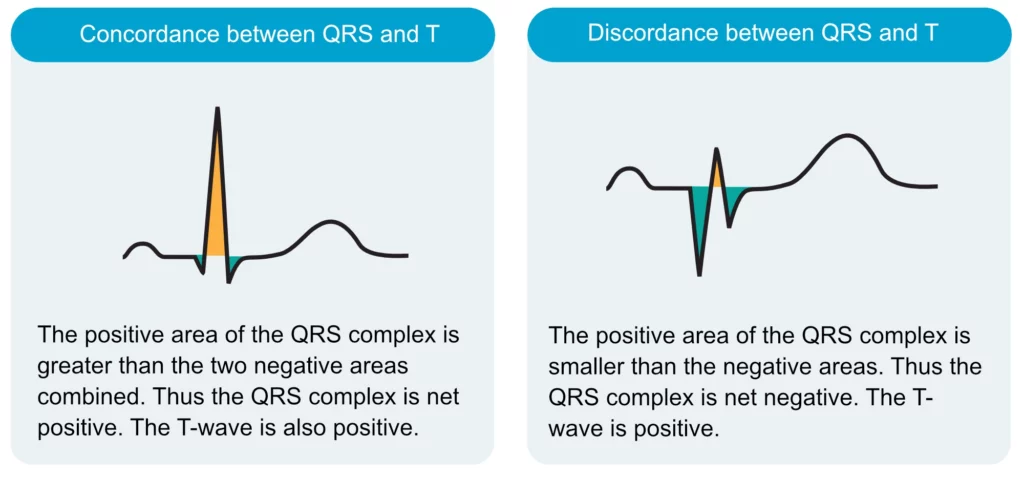
T-bølgen representerer den raske repolarisasjonsfasen (fase 3) av ventrikkelmyokardiet. I et normalt hjerte skal T-bølgen være konkordant med QRS-komplekset, det vil si ha samme retning som QRS-kompleksets nettoretning. Et nettonegativt QRS-kompleks skal følges av en negativ T-bølge, mens et nettopositivt QRS-kompleks skal følges av en positiv T-bølge. Dersom QRS-komplekset og T-bølgen har motsatt retning uten en fysiologisk forklaring, betegnes T-bølgen som diskordant (figur 8), noe som kan indikere patologi som iskemi eller belastning.
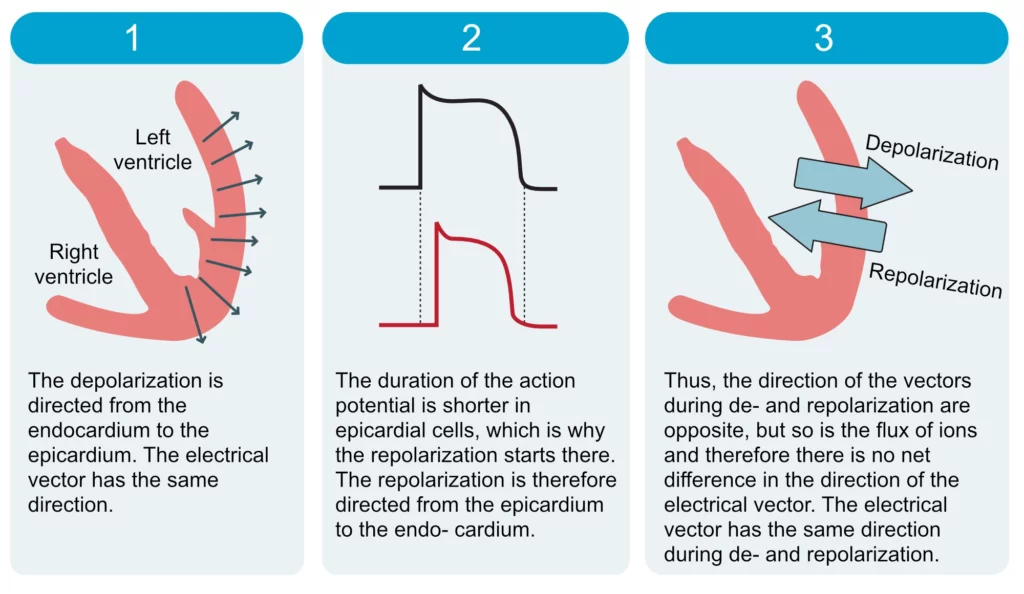
Det kan ved første øyekast virke ulogisk at QRS-komplekset (depolarisering) og T-bølgen (repolarisering) har samme retning på EKG, ettersom ionestrømmene er motsatte (innstrømming av Na⁺/Ca²⁺ vs. utstrømming av K⁺). Intuitivt kunne man forvente at motsatte prosesser ville gi elektriske signaler med motsatt polaritet. Forklaringen ligger i rekkefølgen på hendelsene:
Depolariseringen av den frie ventrikkelveggen forløper fra endokard til epikard. Repolariseringen skjer imidlertid i motsatt retning; den starter i epikard og brer seg mot endokard (figur 9). Dette fenomenet skyldes at epikardiale celler har kortere aksjonspotensialer enn endokardiale celler (en forskjell i fordelingen av kaliumkanaler). Derfor begynner epikardcellene å repolarisere før endokardcellene.
Matematisk betyr dette at siden både (1) ionestrømmenes natur er reversert og (2) retningen på bølgefronten er reversert (dobbelt negativt), blir nettoresultatet positivt på EKG-kurven. T-bølgen vil derfor være rettet i samme retning som QRS-komplekset.
T-bølgevektoren er normalt rettet fremover, lett mot venstre og nedover. Hos barn og ungdom kan den imidlertid være mer orientert mot venstre og bakover («juvenilt T-bølgemønster»), noe som resulterer i negative T-bølger i de høyresidige brystavledningene (V1–V3/V4). Disse normaliseres, det vil si blir positive, i løpet av puberteten. Det er imidlertid verdt å merke seg at en negativ T-bølge i avledning V1 hos voksne er et vanlig funn og samsvarer med QRS-komplekset, som generelt er negativt i V1. En isolert positiv T-bølge i V1 (hos voksne) kan være et patologisk tegn, spesielt hvis T-bølgen i V6 samtidig er negativ.
Til slutt kan vi merke oss morfologiske forskjeller: P- og T-bølgene har en jevn, avrundet form, mens QRS-komplekset er preget av skarpe topper (spikuler). Dette skyldes frekvensinnholdet i signalene; P- og T-bølgene genereres av relativt langsomme endringer i potensialet (lavfrekvente signaler), mens den raske depolariseringen av ventriklene i fase 0 gir QRS-komplekset et høyfrekvent innhold.