Inotrope og vasopressorer: Doser, indikasjoner, kontraindikasjoner og virkninger
Inotrope midler og vasopressorer
Vasopressorer er medikamenter som induserer vasokonstriksjon ved å øke systemisk vaskulær motstand (SVR), noe som primært øker det gjennomsnittlige arterielle trykket (MAP). Inotrope midler øker hjertets kontraktile kraft (positiv inotropi), noe som bedrer slagvolumet og dermed hjerteminuttvolumet (CO). Mange av disse medikamentene påvirker også hjertefrekvensen (kronotropi) og ledningshastigheten (dromotropi).
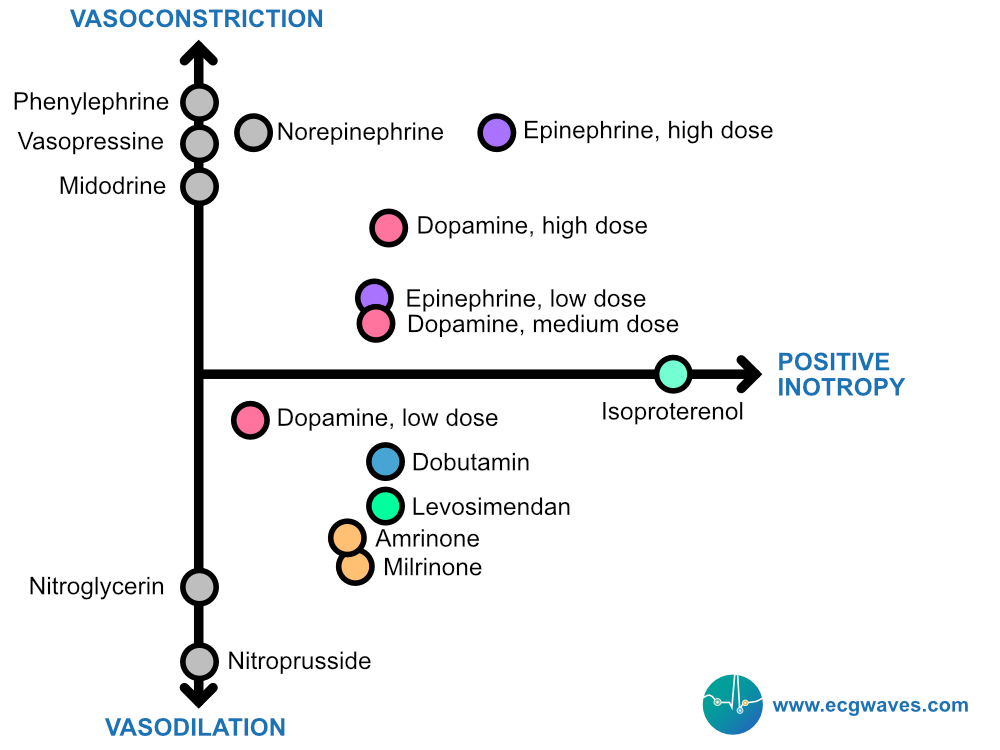
I klinisk praksis, spesielt ved behandling av sirkulatorisk sjokk, er målet å gjenopprette tilstrekkelig organperfusjon. Det finnes flere endogene og syntetiske stoffer som ofte kombineres for å oppnå det ønskede hemodynamiske resultatet. Balansen mellom å øke perfusjonstrykket og å unngå unødig økning i myokards oksygenforbruk ($\text{MVO}_2$) er kritisk. De fleste midlene har både vasopressorisk og inotrop effekt i varierende grad, avhengig av dose og reseptorprofil (figur 1).
Nedenfor følger en medikamentmanual for bruk på koronaravdelingen, intensivavdelingen eller akuttmottaket. Behandling med potente vasoaktive legemidler krever nøye elektrokardiografisk og hemodynamisk overvåking. Minimumsstandard er vanligvis kontinuerlig EKG, pulsoksymetri og invasiv trykkmåling via intraarterielt kateter (arteriekran). Sentralt venekateter (SVK) er ofte nødvendig for trygg administrasjon og for måling av sentralvenøs oksygenmetning ($\text{ScvO}_2$), som gir en indikasjon på balansen mellom oksygentilbud og oksygenforbruk.
Oversikt over vasopressorer og inotrope midler
Tabell 1. Legemiddelmanual for inotrope og vasopressorer
| Legemiddel | Indikasjoner | Dose | α1-effekt | β1-effekt | β2-effekt | D1/D2-effekt | Resultat | Bivirkninger |
|---|---|---|---|---|---|---|---|---|
| Dopamin – lav dose | Sjelden brukt (ingen dokumentert nyrebeskyttende effekt) | Lav dose: 0,5-3,0 μg/kg/min | Lavdose dopamin stimulerer D1-reseptorer og induserer vasodilatasjon i koronar-, nyre-, cerebrale og mesenteriske kar. Klinisk effekt er omdiskutert. | Få | ||||
| Dopamin – middels dose | Kardiogent sjokk Vasodilaterende sjokk Hjertesvikt (HF), akutt Hjertesvikt (HF), kronisk Bradykardi (andrelinjealternativ) |
Middels dose: 3,0-10,0 μg/kg/min. | Middels dose dopamin aktiverer β1, frigjør endogent noradrenalin og øker dermed kontraktilitet, hjertefrekvens (kronotropi) og gir en mild økning i SVR. | Ventrikulære arytmier Myokardiskemi Vevsiskemi (høye doser eller ekstravasasjon) |
||||
| Dopamin – høy dose | Kardiogent sjokk Vasodilaterende sjokk Hjertesvikt (HF), akutt Hjertesvikt (HF), kronisk Bradykardi (andrelinjealternativ) |
Høy dose: 10,0-20,0 μg/kg/min. | Høy dose dopamin induserer i tillegg kraftig α1-stimulering og dermed vasokonstriksjon og uttalt økning i SVR. | Som middels dose, og i tillegg alvorlig hypertensjon (forsiktighet hvis pasienten står på ikke-selektive betablokkere). Økt risiko for arytmier sammenlignet med noradrenalin. | ||||
| Dobutamin | Kardiogent sjokk Akutt hjertesvikt med lavt CO Bradykardi (andrelinjebehandling) Stresstesting (ekkokardiografi) |
Vanlig: 2,0-20 μg/kg/min Maks: 40 μg/kg/min |
0 | Potent inotrop med svak kronotrop effekt (doseavhengig). Doser <5 μg/kg/min induserer mild vasodilatasjon (redusert afterload). Doser >5 μg/kg/min kan gi økt vasokonstriksjon, men nettoeffekten er ofte redusert SVR. |
Takykardi Økt ventrikkelfrekvens ved AF Ventrikulære arytmier Kardiell iskemi (økt MVO2) Hypertensjon (hos pasienter som står på ikke-selektiv β-blokker) Toleranseutvikling (takyfylaksi) etter noen dager (48-72t). |
|||
| Noradrenalin | Sjokk (førstelinje ved septisk, kardiogent og udifferensiert sjokk) Hypotensjon (hvilken som helst) |
0.01-3,0 μg/kg/min
Kan gis perifert i lave doser i kort tid, men SVK foretrekkes. |
0 | Potent vasokonstriktor med mild inotrop effekt. Øker systolisk trykk, diastolisk trykk og pulstrykk med minimal effekt på CO (kan øke CO ved å øke preload via venokonstriksjon, eller redusere CO ved for høy afterload). Minimal kronotrop effekt. Øker koronar perfusjonstrykk. | Refleksbradykardi Atrielle eller ventrikulære arytmier Perifer (digital) iskemi ved høye doser Hypertensjon (spesielt pasienter med ikke-selektive β-blokkere) Langvarig bruk kan være kardiotoksisk. |
|||
| Adrenalin | Sjokk (alle typer – men forsiktighet ved kardiogent) Hjertestans (ACLS) Bronkospasme Anafylaksi (førstevalg) Bradykardi (andrelinjealternativ) |
Infusjon: 0,01 til 0,10 μg/kg/min Bolus 1 mg i.v. hvert 3. til 5. minutt (maks. 0,2 mg/kg) ved stans. i.m.: (1:1000): 0.3 til 0,5 mg (voksne) Trygt for perifer bruk (i.m. eller akutt i.v.) |
N/A | Beta-effekt mer uttalt ved lave doser (økt CO og HF). Alfa-effekt mer uttalt ved høyere doser (vasokonstriksjon). Økt koronar gjennomstrømning. Pulmonal vasokonstriksjon. Øker laktatproduksjon (glykogenolyse/aerob glykolyse). |
Ventrikulære arytmier Alvorlig hypertensjon som resulterer i cerebrovaskulær blødning Kardiell iskemi (kraftig økning i MVO2) Plutselig hjertedød Hyperlaktatemi (type B) uten hypoksi. |
|||
| Isoproterenol (Isoprenalin) | Bradykardi (førstelinjebehandling ved hemodynamisk betydning) Bradykardi som forårsaker torsade de pointes (øker hjertefrekvensen og forkorter QT) Brugadas syndrom (elektrisk storm) |
0.5-10,0 μg/min (merk: dosering i μg/min, ikke kg) Trygt for perifer bruk |
0 | 0 | Kraftig kronotrop og inotrop effekt. Potent systemisk vasodilatasjon (β2). Mild pulmonal vasodilatasjon. Nettoeffekt ofte økt CO, men redusert MAP pga fall i SVR. | Ventrikulære arytmier Kardiell iskemi (høyt oksygenforbruk) Hypertensjon (systolisk) Hypotensjon (diastolisk) |
||
| Fenylefrin | Brukes vanligvis som akutt bolus for å korrigere akutt hypotensjon (f.eks. ved anestesiinnledning). Hypotensjon (hvilken som helst) Brukes for å øke MAP under hypotensjon ved aortastenose (unngår takykardi). Brukes for å redusere LVOT-gradienten ved HCM Brukes til å korrigere hypotensjon forårsaket av samtidig inntak av sildenafil og nitrater |
Bolus: 50 til 100 µg IV (titreres) Infusjon: 0,4 til 9,1 μg/kg/min Trygt for perifer bruk |
0 | 0 | N/A | Ren α1-agonist. Umiddelbar og uttalt økning i SVR og MAP. Ingen direkte effekt på hjertet, men øker afterload. | Refleksbradykardi (via baroreseptorer) Hypertensjon Redusert CO (pga økt afterload) Alvorlig perifer og visceral vasokonstriksjon Vevsnekrose ved ekstravasasjon |
|
| Milrinon (fosfodiesterasehemmer) | Hjertesvikt, akutt Hjertesvikt, dekompensert kronisk Høyre ventrikkelsvikt / Pulmonal hypertensjon |
Bolus: Unngås ofte for å forhindre hypotensjon (evt 50 μg/kg over 10-30 min) Infusjon: 0,375 til 0,75 μg/kg/min. |
0 | 0 | 0 | 0 | PDE3-hemmer (fosfodiesterasehemmer). Potent inotropt middel («inodilatator»). Induserer vasodilatasjon i systemiske og pulmonale kar. Resulterer i redusert preload, afterload og SVR, med økt CO. |
Ventrikulære arytmier Hypotensjon (krever ofte samtidig noradrenalin) Myokardisk iskemi Akkumuleres ved nyresvikt (dosejustering nødvendig, lang halveringstid) |
| Amrinon | Hjertesvikt, akutt Hjertesvikt, dekompensert kronisk |
Bolus 0.75 mg/kg over 2 til 3 min Infusjon: 5 til 10 μg – kg-1 – min-1 | 0 | 0 | 0 | 0 | PDI (fosfodiesterasehemmer). Brukes sjelden/aldri klinisk lenger på grunn av bivirkningsprofil (trombocytopeni). Milrinon foretrekkes. | Arytmier, forsterket AV-overledning Hypotensjon Trombocytopeni (doseavhengig) Hepatotoksisk |
| Vasopressin | Septisk sjokk (andrelinje) Vasodilaterende sjokk (f.eks. post-cardiotomy) Hjertestans (ikke lenger i standard algoritme, men kan vurderes) |
Infusjon: 0,01-0,03 U/min (fast dose, titreres sjelden)
Bolus (IV): 40 U (ved stans – foreldet) |
0 | 0 | 0 | 0 | Vasopressin stimulerer V1-reseptorer (glatt muskulatur i karene) og V2-reseptorer (nyrene). V1-stimulering induserer vasokonstriksjon. Vasopressin øker SVR uten signifikant inotropi eller kronotropi. «Sparer» katekolaminer. Effektiv ved acidose der katekolaminer mister effekt. | Arytmier (men mindre enn katekolaminer) Hypertensjon Redusert CO (ved doser >0,04 U/min) Kardial iskemi Alvorlig perifer vasokonstriksjon som forårsaker iskemi (spesielt hud/fingre) Splanchnisk vasokonstriksjon |
| Levosimendan | Hjertesvikt, dekompensert kronisk Kardiogent sjokk (spesielt ved iskemisk etiologi eller ved betablokker-behandling) |
Ladningsdose: 6-12 μg/kg (unngås ofte ved hypotensjon) Infusjon: 0,05-0,2 μg/kg/min i 24 timer. |
0 | 0 | 0 | 0 | Levosimendan er en kalsiumsensibilisator som øker myofilamentenes følsomhet for kalsium (økt kontraktilitet uten økt kalsiuminflux). Åpner K-ATP-kanaler (vasodilatasjon). Langvarig effekt (aktive metabolitter i opptil 7-9 dager). | Forbedret AV-overledning (kan gi AF) Hypotensjon (vasodilatasjon) Hodepine Hypokalemi |
Klinisk anvendelse ved ulike sjokktilstander
Valg av vasoaktivt medikament bør baseres på den underliggende fysiologiske forstyrrelsen. En grundig klinisk vurdering supplert med ekkokardiografi er essensielt for å kategorisere sjokket.
- Septisk sjokk: Karakteriseres av lav SVR (vasodilatasjon). Noradrenalin er førstevalg for å øke MAP (>65 mmHg). Ved behov for høye doser noradrenalin (ofte definert som >0,25–0,5 µg/kg/min) bør Vasopressin legges til som andrelinjevalg for å redusere katekolaminbelastningen og utnytte synergistisk effekt. Ved ledsagende myokarddepresjon kan dobutamin vurderes i tillegg.
- Kardiogent sjokk: Karakteriseres av lavt CO og (vanligvis) høy SVR. Målet er å bedre pumpefunksjonen uten å øke afterload eller oksygenforbruk uhensiktsmessig.
- Noradrenalin foretrekkes ofte fremfor dopamin ved hypotensjon, da det gir færre arytmier (ref. SOAP II-studien).
- Dobutamin er førstevalg som inotrop støtte, men kan gi hypotensjon og arytmier.
- Levosimendan kan være fordelaktig hos pasienter som bruker betablokkere, da effekten er uavhengig av beta-reseptorer.
- Milrinon er et godt alternativ ved samtidig pulmonal hypertensjon og høyresidig svikt, men krever årvåkenhet for hypotensjon.
- Anafylaktisk sjokk: Adrenalin er absolutte førstevalg (i.m. initialt, i.v. titrert ved refraktær sjokk) da det reverserer bronkospasme og vasodilatasjon samtidig som det øker kontraktiliteten.
Fysiologi: Reseptorer for katekolaminer
Forståelsen av reseptorprofilen er nøkkelen til presis titrering. Merk at selektiviteten ofte er doseavhengig; ved svært høye doser mister mange midler sin reseptorselektivitet.
- Alfa-1-adrenerge reseptorer (α1): Finnes hovedsakelig i glatte muskelceller i blodårene (arterioler og vener). Aktivering via G-protein-koblede reseptorer fører til økt intracellulært kalsium og dermed vasokonstriksjon og økt SVR. Dette øker blodtrykket, men kan redusere organperfusjon ved overdreven konstriksjon.
- Beta-1-adrenerge reseptorer (β1): Dominerende reseptor i myokardiet (både ledningssystemet og arbeidsmyokard). Stimulering øker cAMP-nivået, noe som resulterer i:
- Positiv inotropi (økt kontraktil kraft).
- Positiv kronotropi (økt hjertefrekvens).
- Positiv dromotropi (økt ledningshastighet).
- Beta-2 adrenerge reseptorer (β2): Uttrykkes i vaskulære glatte muskelceller (særlig i skjelettmuskulatur og koronarkar) og i bronkiene. Stimulering fører til avslapning av glatt muskulatur (vasodilatasjon og bronkodilatasjon). Dette kan gi et fall i diastolisk blodtrykk.
- Dopaminerge reseptorer (D1 og D2): D1-reseptorer finnes i nyre-, mesenteriske, koronare og cerebrale kar. Stimulering gir vasodilatasjon. D2-reseptorer finnes presynaptisk og hemmer frigjøring av noradrenalin. Klinisk nytte av «nyredose» dopamin er ikke dokumentert og anbefales ikke lenger for nyreproteksjon.
NB: Raske blodtrykksendringer kan indusere refleksive autonome responser (baroreseptorrefleks) som påvirker det endelige hemodynamiske resultatet. For eksempel kan ren α1-stimulering med fenylefrin gi en refleksbradykardi som reduserer CO, til tross for økt MAP.
Dobutamin er et syntetisk katekolamin utviklet for å maksimere inotrop effekt med mindre perifer vasokonstriksjon enn dopamin og noradrenalin.
Referanser
- Overgaard, Dzavik et al. Inotrope og vasopressorer: Gjennomgang av fysiologi og klinisk bruk ved hjerte- og karsykdommer. Circulation 2011.
- Jentzer et al. Pharmacotherapy Update on the Use of Vasopressors and Inotropes in the Intensive Care Unit. J Cardiovasc Pharmacol Therap (2014).
- Müllner M, Urbanek B, Havel C, et al. Vasopressorer mot sjokk. Cochrane Database Syst Rev 2004
- Ballieu P, Besharatian Y, Ansari S. Safety and Feasibility of Phenylephrine Administration Through a Peripheral Intravenous Catheter in a Neurocritical Care Unit. J Intensive Care Med 2021; 36:101.
- Lherm T, Troché G, Rossignol M, et al. Nyreeffekter av lavdose dopamin hos pasienter med sepsis syndrom eller septisk sjokk behandlet med katekolaminer. Intensive Care Med 1996; 22:213.
- Unverferth DA, Blanford M, Kates RE, Leier CV. Toleranse for dobutamin etter 72 timers kontinuerlig infusjon. Am J Med 1980; 69:262.
- Gattinoni L, Brazzi L, Pelosi P, et al. En studie av målorientert hemodynamisk terapi hos kritisk syke pasienter. SvO2 Collaborative Group. N Engl J Med 1995; 333:1025.
- Gregory JS, Bonfiglio MF, Dasta JF, et al. Erfaring med fenylefrin som en komponent i den farmakologiske støtten av septisk sjokk. Crit Care Med 1991; 19:1395.
- De Backer D, Creteur J, Silva E, Vincent JL. Effekter av dopamin, noradrenalin og adrenalin på den splanchniske sirkulasjonen ved septisk sjokk: hva er best? Crit Care Med 2003; 31:1659.
- MacGregor DA, Smith TE, Prielipp RC, et al. Farmakokinetikk av dopamin hos friske mannlige forsøkspersoner. Anesthesiology 2000; 92:338.
- Löllgen H, Drexler H. Bruk av inotrope midler i intensivbehandling. Intensivmedisin 1990; 18:S56.
- Steel, A, Bihari, D . Valg av katekolamin: spiller det noen rolle? Curr Opin Crit Care 2000; 6:347.
- Hannemann L, Reinhart K, Grenzer O, et al. Sammenligning av dopamin med dobutamin og noradrenalin for oksygentilførsel og -opptak ved septisk sjokk. Crit Care Med 1995; 23:1962.
- Al-Hesayen A, Azevedo ER, Newton GE, Parker JD. Effekten av dobutamin på hjertets sympatiske aktivitet hos pasienter med kongestiv hjertesvikt. J Am Coll Cardiol 2002; 39:1269.
- De Backer D, Biston P, Devriendt J, et al. Sammenligning av dopamin og noradrenalin i behandlingen av sjokk. N Engl J Med 2010; 362:779.
- Mutlu GM, Factor P. Vasopressins rolle i behandlingen av septisk sjokk. Intensive Care Med 2004; 30:1276.
- Sharshar T, Blanchard A, Paillard M, et al. Sirkulerende vasopressinnivåer ved septisk sjokk. Crit Care Med 2003; 31:1752.
- Tsuneyoshi I, Yamada H, Kakihana Y, et al. Hemodynamiske og metabolske effekter av lavdose vasopressininfusjoner ved vasodilaterende septisk sjokk. Crit Care Med 2001; 29:487.
- Dünser MW, Mayr AJ, Ulmer H, et al. Arginin vasopressin ved avansert vasodilaterende sjokk: en prospektiv, randomisert, kontrollert studie. Sirkulasjon 2003; 107:2313.
- Kill C, Wranze E, Wulf H. Vellykket behandling av alvorlig anafylaktisk sjokk med vasopressin. To kasuistikker. Int Arch Allergy Immunol 2004; 134:260.
- Schummer C, Wirsing M, Schummer W. Vasopressins sentrale rolle ved refraktært anafylaktisk sjokk. Anesth Analg 2008; 107:620.
- McIntyre WF, Um KJ, Alhazzani W, et al. Association of Vasopressin Plus Catecholamine Vasopressors vs Catecholamines Alone With Atrial Fibrillation in Patients With Distributive Shock: A Systematic Review and Meta-analysis. JAMA 2018; 319:1889.
- Albanèse J, Leone M, Delmas A, Martin C. Terlipressin eller noradrenalin i hyperdynamisk septisk sjokk: en prospektiv, randomisert studie. Crit Care Med 2005; 33:1897.
- Kam PC, Williams S, Yoong FF. Vasopressin og terlipressin: farmakologi og klinisk relevans. Anestesi 2004; 59:993.
- O’Brien A, Clapp L, Singer M. Terlipressin for noradrenalinresistent septisk sjokk. Lancet 2002; 359:1209.
- Leone M, Albanèse J, Delmas A, et al. Terlipressin hos katekolaminresistente pasienter med septisk sjokk. Sjokk 2004; 22:314.
- Rodríguez-Núñez A, Fernández-Sanmartín M, Martinón-Torres F, et al. Terlipressin for katekolaminresistent septisk sjokk hos barn. Intensive Care Med 2004; 30:477.
- Morelli A, Rocco M, Conti G, et al. Effekter av terlipressin på systemisk og regional hemodynamikk ved katekolaminbehandlet hyperkinetisk septisk sjokk. Intensive Care Med 2004; 30:597.
- Polito A, Parisini E, Ricci Z, et al. Vasopressin for behandling av vasodilatorisk sjokk: en ESICM systematisk gjennomgang og metaanalyse. Intensive Care Med 2012; 38:9.
- Gordon AC, Mason AJ, Thirunavukkarasu N, et al. Effekt av tidlig vasopressin vs noradrenalin på nyresvikt hos pasienter med septisk sjokk: The VANISH Randomized Clinical Trial. JAMA 2016; 316:509.
- Malay MB, Ashton JL, Dahl K, et al. Heterogenitet av vasokonstriktoreffekten av vasopressin i septisk sjokk. Crit Care Med 2004; 32:1327.
- Kahn JM, Kress JP, Hall JB. Hudnekrose etter ekstravasasjon av lavdose vasopressin administrert for septisk sjokk. Crit Care Med 2002; 30:1899.
- Leather HA, Segers P, Berends N, et al. Effekter av vasopressin på høyre ventrikkelfunksjon i en eksperimentell modell av akutt pulmonal hypertensjon. Crit Care Med 2002; 30:2548.
- Dünser MW, Mayr AJ, Tür A, et al. Iskemiske hudlesjoner som en komplikasjon av kontinuerlig vasopressininfusjon ved katekolaminresistent vasodilaterende sjokk: forekomst og risikofaktorer. Crit Care Med 2003; 31:1394.
- Russell JA, Walley KR, Singer J, et al. Vasopressin versus noradrenalininfusjon hos pasienter med septisk sjokk. N Engl J Med 2008; 358:877.
- Jeon K, Song JU, Chung CR, et al. Forekomst av hypotensjon i henhold til seponeringsrekkefølgen av vasopressorer i behandlingen av septisk sjokk: en prospektiv randomisert studie (DOVSS). Crit Care 2018; 22:131.
- Evans L, Rhodes A, Alhazzani W, et al. Surviving Sepsis Campaign: Internasjonale retningslinjer for behandling av sepsis og septisk sjokk 2021. Crit Care Med 2021; 49:e1063.
- Landoni G, Lomivorotov VV, Alvaro G, et al. Levosimendan for hemodynamisk støtte etter hjertekirurgi. N Engl J Med 2017.
- Mehta RH, Leimberger JD, van Diepen S, et al. Levosimendan hos pasienter med dysfunksjon i venstre ventrikkel som gjennomgår hjertekirurgi. N Engl J Med 2017.
- Khanna A, English SW, Wang XS, et al. Angiotensin II for behandling av vasodilaterende sjokk. N Engl J Med 2017; 377:419.